近年、新薬の登場などで
大きく進歩しているがん治療。
既存の薬や治療法との組み合わせを含めた、
より有効な治療法を確立するために、
いま臨床試験・治験の重要性が高まっています。
患者、そして市民がともに
未来のがん治療を“共創”する時代へ。
がん医療の専門家と一緒に、
臨床試験・治験や「患者・市民参画」の
大切さを考えてみませんか。
インタビューinterview
がんの治療の臨床試験に市民のアイデアを反映させる取り組みが進んでいます。「患者・市民参画」(PPI)と呼ばれています。国内190もの医療機関が参加する日本臨床腫瘍研究グループ(JCOG)はその先陣役。公益財団法人「日本対がん協会」と臨床試験の参加に向けた知識を備えてもらおうと、動画も公開しました。JCOG運営事務局長の中村健一さん(医師)が語る日本が置かれているがん治療の現状とは。

- 中村 健一(なかむら・けんいち) 国立がん研究センター中央病院 国際開発部門長
- 京都大学医学部卒業後、消化器外科医として臨床経験を積み、2006年から国立がん研究センター中央病院でJCOGの運営、管理にあたる。2015年から同病院で医師主導治験の支援部門を立ち上げ、様々な新規プロジェクトを手掛けている。2020年から厚労省、AMEDの支援のもと、アジア臨床試験ネットワーク事業をプロジェクトリーダーとして率いるとともに、臨床研究法やICH-GCP改正などに関する厚労省研究班で中心的な役割を果たしている。
――技術開発の進展で、2000年代に入って多くの新しい薬が登場しました。
正常な細胞とがん細胞といずれも攻撃するそれ以前の抗がん剤と異なり、がんの原因となっている特定の分子を標的にがん細胞だけを狙い撃ちする「分子標的薬」が登場し、2010年代には多くの新しい分子標的薬が登場しました。
――2010年代には、京都大学の本庶佑氏がノーベル賞を受けて関心を集めた免疫チェックポイント阻害薬も登場しましたね。
本庶さんらが開発したのは小野薬品工業の「オプジーボ」ですね。その後もほかの免疫チェックポイント阻害薬の開発も続きました。ほかにも新しい手法で開発した治療薬が出てきて、製薬企業の開発競争はさらに激しくなりました。
――ここ数年はがん細胞の遺伝子的な特徴をターゲットにして薬を使う治療法も盛んになりましたね。
昔は肺がんならこの薬、乳がんならこの薬と、がん種ごとに薬や臨床試験が区分けされていました。しかし、こうした区分けはどんどん細分化されていっています。一口に肺がんといっても、遺伝子レベルでみると、その特徴の違いは無数にあります。その特徴ごとに応じてがん細胞を攻撃する治療薬の開発が主流になっています。
――がんの多くに見られる特徴をターゲットにする試験が優先されませんか。
企業の臨床試験は、売り上げのためにまとまった患者数が見込めるがん細胞の特徴をターゲットにした治療薬の開発をどうしても優先する傾向にあります。これに伴い、同じ種類のがんでも、治療薬に結びつく特徴を持つがんと、そうでないがんが生じることになります。
――細分化が進めば進むほど、それ以外のがん細胞の特徴がある患者への治験はされず、置き去りにされていくことになるわけですね。
そうしたがんに加えて、希少がんについてもなかなか開発が進まなかったため、その対策として2003年に、法律が改正されて、それまで製薬企業しかできなかった治療薬の承認を得るための臨床試験(治験)を、医師が企画・立案して取り組むことができるようになりました。「医師主導治験」と呼ばれています。企業ができない、あるいはやらない分野の治験へのニーズが高まったことも背景にあると思います。
――欧米など先進諸国よりも承認に時間がかかり導入が遅れる「ドラッグラグ」や、そもそも日本にずっと入ってこない状態が続く「ドラッグロス」という問題が指摘されています。
近年は海外の新興バイオ医薬品企業(Emerging Biopharma=EBP)が治療薬の開発を担うことが多くなっています。ベンチャーなので大手の製薬企業より人材や資金が限られ、特定の市場での開発を優先することから、まず欧米で治験をする例が目立っています。日本の市場はどうしても後回しになりがちです。
――日本の市場は魅力がないということなのでしょうか。
日本は毎年、薬価が改定されるなど、価格が下げられるリスクがあります。米国のように、企業が薬価を決められないので、企業としては売り上げを予想して投資がしにくい環境です。そのうえ人口も減ることが予想されています。治験の手続きには日本語も必要なことなどが壁になっていると思います。
――患者のためになるけど、企業がやらないような臨床試験って、どんな臨床試験ですか。
たとえば、手術の前と後のどちらの時期に抗がん剤治療をしたらよいかを比べる試験。製薬企業にとっては売り上げに関係ないのでどちらでもいいわけですが、食道がんでは手術の前に抗がん剤治療をする方が良いことが臨床試験でわかりました。薬の量や使う期間を減らす臨床試験も同じで、売り上げには寄与しませんが、患者にとっては副作用や経済的負担が減るという大きなメリットがあります。
――患者にとって負担は軽くなりますが、製薬企業にとっては売り上げが減ることになりますね。
ライバル社の薬剤の直接比較も、患者にとってはどっちの薬がいいのか知りたいのは当然ですが、製薬企業にとっては大きく売り上げに影響するリスクを負うことになる試験です。そうした企業があまりやらないけれど、患者さんにとってニーズの高い研究を実施するのがJCOGの使命です。
――臨床試験の企画段階から患者にアイデアを出してもらう取り組みも始まっていると聞きました。
以前にJCOGで乳がんの手術をやめることができるかどうかを調べる試験を検討し、患者の方々に意見を聞いたことがあります。そのときに驚いたのは、手術よりも、術後のホルモン療法の負担が大きいために、そのホルモン療法をしないでもよい方法を見つける試験をしてほしいと要望されたことです。患者さんが苦痛だと感じていることは、ひとつではなく多様であることに気づかされました。
――JCOGは2018年から「患者参画小委員会」を立ち上げました。
患者との意見交換会や、臨床試験について学んでもらうセミナーの開催などをしています。今回、対がん協会と一緒につくった動画は、いわばこの初級編です。臨床試験の基本的なことが学べ、ご自身やご家族、友人などががんになったときの備えにもなります。多くの方に患者市民参画の導入口として見てもらえたらと思います。
(聞き手 服部尚・日本対がん協会検診研究グループマネジャー)
- JCOG
- 1978年に開始された厚生労働省の「がんの集学的治療の研究」班を前身に、1990年に、日本臨床腫瘍研究グループ(JCOG)と命名され、多施設共同研究グループとしてスタートした。がんの標準治療の確立を目的として研究活動を進めている。全国約190医療機関、計約700の診療科が所属している。
動画で学ぶmovie
公益財団法人日本対がん協会は2022年12月に全国190の医療機関が参加してがん医療の臨床試験を進める日本臨床腫瘍研究グループ(JCOG)との共催で、公開講座「私たちも一緒に作る、がん最新治療 未来のがん治療のこと みんなで考えよう~臨床試験を身近に~」をオンライン開催しました。公開講座にはがん患者や家族、医師や看護師などの医療関係者からメディア関係者まで、幅広い分野から924人が参加。市民や患者の立場から、がん医療づくりに参加するために必要な知識を各分野の専門家がわかりやすく解説しました。

動画をご覧になって、臨床試験と「患者・市民参画」の大切さを一緒に考えてみませんか。
動画
-

- 「臨床試験、治験とは?」片山 宏 先生
- (国立がん研究センター中央病院 臨床研究支援部門 研究企画推進部 多施設研究支援室 室長/JCOG運営事務局長補佐)
-

- 「臨床試験についての用語を知る(ランダム化、標準治療、など)」山本 精一郎 先生
- (静岡社会健康医学大学院大学教授/国立がん研究センター がん対策研究所 特任研究員)
-

- 「治験、臨床試験の探し方」柴田 大朗 先生
- (国立がん研究センター 研究支援センター 生物統計部 部長)
-

- 「治験、臨床試験に参加したらどんな感じ?」上野 誠 先生
- (神奈川県立がんセンター消化器内科部 部長/JCOG患者参画委員会 副委員長)
-

- 「臨床試験グループ(JCOG)の役割」福田 治彦 先生
- (国立がん研究センター中央病院 臨床研究支援部門 データ管理部 部長/JCOGデータセンター長)
-

- 「JCOGにおける患者市民参画」丸山 大 先生
- (公益財団法人がん研究会有明病院 血液腫瘍科部長、先進がん治療開発センター長/JCOGリンパ腫グループ事務局/JCOG患者参画委員会 委員長)
-

- 「治験に参加し、繋いだ命」青山 政弘 さん
- (ソニー生命保険株式会社)
-

- 司会・進行米盛 勧 先生
- (国立がん研究センター中央病院 腫瘍内科 科長)
-

- 司会・進行大友 明子 さん
- (乳がん患者支援団体メンタル・スパ代表/BEC乳がん体験者コーディネーター/認定心理士)
参加者の声voice
公開講座に参加して「臨床試験」についての理解は深まりましたか?
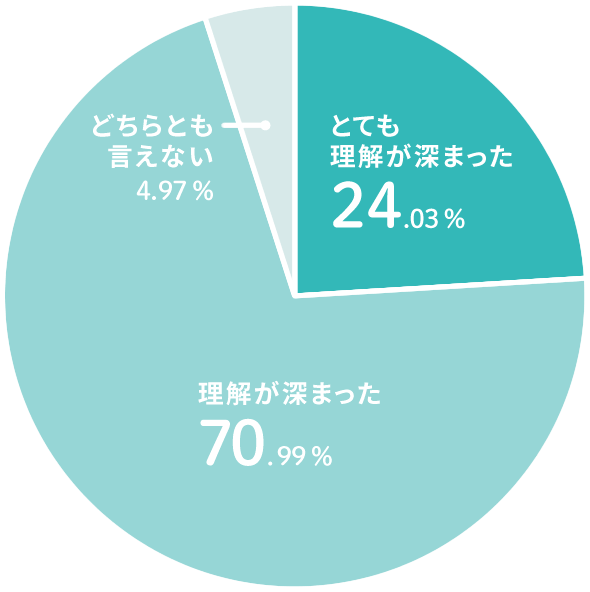
- お試し、犠牲のイメージがあったが、払しょくされた。
- 治験は特別な人だけが受けられるものと思っていたが、自分にも可能性があるとわかった。
- 標準治療ではないことは分かっていたが、もっと有効的であればそれが標準治療になっていくという、常にこうやって医学が進歩していることがよくわかった。
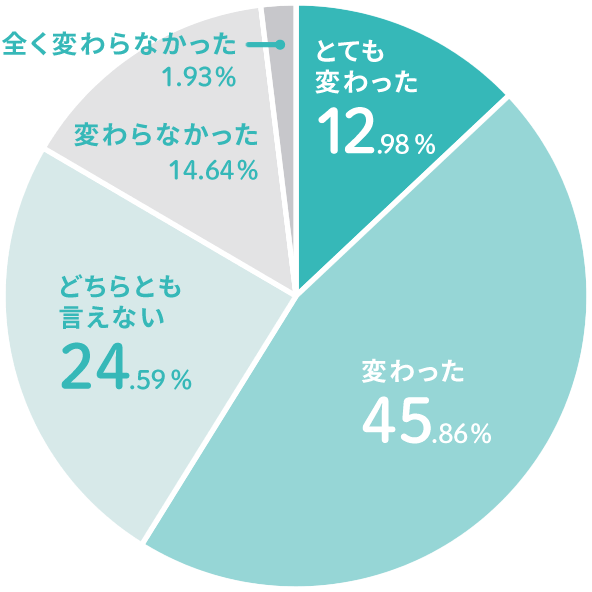
公開講座に参加して「臨床試験」についてお持ちのイメージに変化はありましたか?
- 標準治療をしながら治験するというのは初めて知りました。
- 治療に薬メーカーができる範囲、医療機関ができる範囲がわかれていることは知っていましたが、申請までの詳しい流れが本セミナーでよくわかりました。
- 現在、標準治療を行っていますが治験を紹介されれば利用したいです。
公開講座に参加して「患者参画」について、理解は深まりましたか?
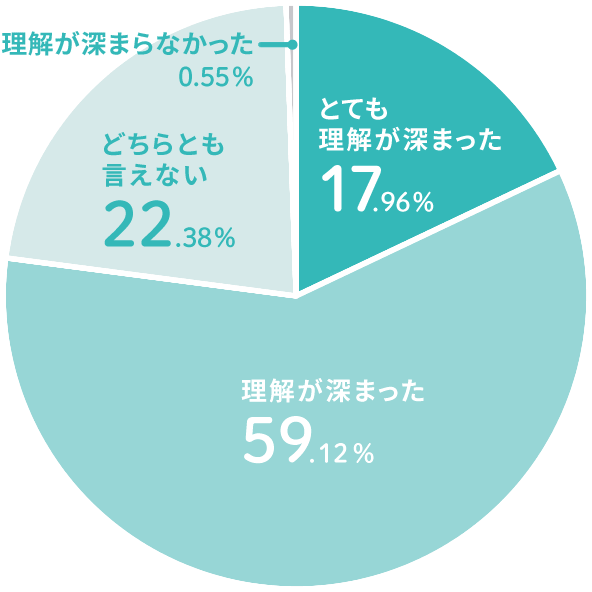
- 患者・医療実施者共同で進める大切さがわかった。
- 治療に薬メーカーができる範囲、医療機関ができる範囲がわかれていることは知っていましたが、申請までの詳しい流れが本セミナーでよくわかりました。
- 患者市民参画に目を向けることが無かったので、参考となった。



